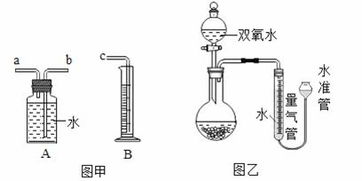
双氧水制取氧气
双氧水在化学中,实验室制取氧气有三种方法:(1)2KMnO4 =加热= K2MnO4 + MnO2 + O2 (2)2KClO3 =MnO2、加热= 2KCl + 3O2 (3)2H2O2 =MnO2= 2H2O + O2 双氧水,就是过氧化氢(H2O2)溶液,其制取氧气的反应原理是上。
双氧水制取氧气的过程和注意事项
要具体的.追加分数总结:若固体(或固体+固体)加热生成气体,选用高锰酸钾制氧气装置;若固体+液体常温下制取气体,选用双氧水制取氧气装置。
催化剂:在化学反应中能改变其他物质的反应速率,但本身的化学性质和质量在反应前后没有发生变化的物质。
过氧化氢制取氧气的化学方程式
过氧化氢制取氧气的化学方程式:2H₂O₂(MnO₂催化剂)=2H₂O+O₂↑ 过氧化氢:化学式为H₂O₂,其水溶液俗称双氧水,外观为无色透明液体,是一种强氧化剂。
过氧化氢在常。
过氧化氢怎么制取氧气
过氧化氢化学式为H2O2,纯过氧化氢是淡蓝色的黏稠液体,可任意比例与水混溶,是一种强氧化剂,水溶液俗称双氧水,为无色透明液体。
其水溶液适用于医用伤口消毒及环境消毒和食品消毒。
在一般情况下会缓慢分解成水和氧气,但。
双氧水制氧气的原理
双氧水分解的原理有很多种,且存有争议,这里介绍一下比较简单的光催化和中学常用的金属催化。
光催化[1]:HOOH==光==2HO·(羟基自由基)HOOH+HO· → HOO·+H2O HOO· + HO· → O2+H2O 金属催化[2]:HOOH+M。
